Chemistry Learner
Dusitan draselný reprezentovaný chemickým vzorcem KNO2 je žlutavě bílý krystalický a rozpuštěný prášek, který je rozpustný ve vodě, alkoholu a kapalném amoniaku . Je to draselná sůl a iontová sloučenina . KNO2 je silným oxidačním činidlem a je neslučitelný se silnými kyselinami, silnými redukčními činidly, kyanidy, amonnými solemi a hořlavými materiály .

Dusitan draselný
Dusitan draselný Identifikace |
|
| Číslo CAS | 7758-09-.0 |
| PubChem CID | 516910 |
| ChemSpider ID | 22857 |
| EC Number | 231-832-4 |
Jak ho vyrobit
Dusitan draselný lze připravit zahříváním dusičnanu draselného s olovem.
KNO3 + Pb = KNO2 + PbO
Pokud chcete, můžete místo olova použít zinek nebo měď .

Vzorec dusitanu draselného
Vlastnosti a charakteristika dusitanu draselného
Všeobecné vlastnosti |
|
| Molární hmotnost/molekulová hmotnost | 85 .103 g/mol |
Fyzikální vlastnosti |
|
| Barva/vzhled | Bílé nebo slabě žluté krystaly |
| Teplota tání/teplota tuhnutí | 441 °C, 825.8°F |
| Teplota varu | 537°C, 998,6°F |
| Hustota | 1.9 g cm-3 |
| Stav hmoty při pokojové teplotě (normální fáze) | Tvrdá látka |
| Tepelná kapacita | 107.4 J/mol K |
| Měrná hmotnost | 1.915 |
Chemické vlastnosti |
|
| Hořlavost | Ano. |
| Rozpustnost ve vodě | 3120 g/l (při 25oC) |
| pH | 8.40 (zásaditá) |
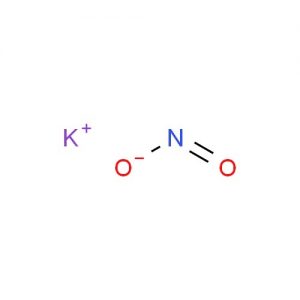
Dusitan draselný Struktura
Podstatné reakce
Reakcí mezi dusitanem draselným a koncentrovanou kyselinou dusičnou vzniká dusičnan draselný, oxid dusičitý, oxid dusnatý a voda .
2KNO2 + 2HNO3 = 2KNO3 + NO2 + NO + H2O
Nasycený roztok KNO2 reaguje s koncentrovanou kyselinou sírovou za vzniku síranu draselného, oxidu dusičitého, oxidu dusnatého a vody .
2KNO2 + H2SO4 = K2SO4 + NO2 + NO + H2O
Dusitan draselný reaguje s koncentrovanou kyselinou chlorovodíkovou za vzniku dusičnanu draselného, chloridu draselného, oxidu dusnatého a vody .
3KNO2 + 2HCl = KNO3 + 2KCl + 2NO + H2O
Použití dusitanu draselného
- K výrobě dalších chemických látek, solí pro přenos tepla .
- V chemické analýze .
- Jako potravinářská přísada (konzervant), v hnojivech .
- Jako protilátka při otravě kyanidem .
- Jako vasodilatátor v lékařství .
- Jako prostředek proti usazování vodního kamene a inhibitor koroze .
Je nebezpečný
Při požití je jedovatý. Při zahřátí může způsobit nebezpečí výbuchu. Sloučenina se začíná rozkládat při 350 °C a uvolňuje toxické výpary oxidu draselného. KNO2 v potravinách může zvýšit riziko vzniku rakoviny .
Cena dusitanu draselného
10 gramů sloučeniny stojí přibližně 19,2 USD.
- Dusitan draselný – Pubchem.ncbi.nlm.nih.gov
- Dusitan draselný – Chemspider.com
- Jaké je pH 0,25M roztoku dusitanu draselného? – Quora.com
- Dusitan draselný – Chemicalbook.com
- Příprava dusitanu draselného – Prepchem.com
- Dusitan draselný – Chemicalbook.com
- Dusitan draselný reaguje s kyselinou dusičnou – Chemiday.com
- Dusitan draselný reaguje s kyselinou sírovou – Chemiday.com
- Dusitan draselný reaguje s chlorovodíkem – Chemiday.com
.