Chemistry Learner
Kaliumnitriet vertegenwoordigd door de chemische formule KNO2 is een geelachtig wit kristallijn en vervloeiend poeder dat oplosbaar is in water, alcohol en vloeibare ammoniak . Het is een kaliumzout en een ionische verbinding. KNO2 is een sterk oxidatiemiddel en onverenigbaar met sterke zuren, sterke reductiemiddelen, cyaniden, ammoniumzouten en brandbare materialen .

Kaliumnitriet
Kaliumnitriet Identificatie |
|
| CAS Nummer | 7758-09-0 |
| PubChem CID | 516910 |
| ChemSpider ID | 22857 |
| EC Nummer | 231-832-4 |
Hoe te maken
Kaliumnitriet kan worden bereid door kaliumnitraat te verhitten met lood.
KNO3 + Pb = KNO2 + PbO
Als je wilt, kun je zink of koper gebruiken in plaats van lood.

Kaliumnitriet formule
Eigenschappen en kenmerken van kaliumnitriet
Algemene eigenschappen |
|
| Molaire massa/moleculair gewicht | 85.103 g/mol |
Fysische eigenschappen |
|
| Kleur/uiterlijk | Witte of lichtgele kristallen |
| Smeltpunt/vriespunt | 441°C, 825.8°F |
| kookpunt | 537°C, 998.6°F |
| dichtheid | 1.9 g cm-3 |
| Staat van de materie bij kamertemperatuur (normale fase) | Vast |
| Warmtecapaciteit | 107.4 J/mol K |
| Specifieke zwaartekracht | 1.915 |
Chemische eigenschappen |
|
| Ontvlambaarheid | Ja |
| Oplosbaarheid in water | 3120 g/l (bij 25oC) |
| pH | 8.40 (basisch) |
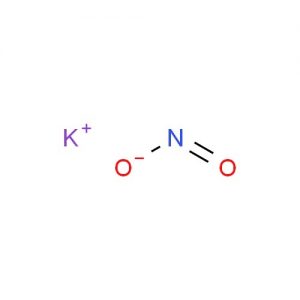
Kaliumnitriet Structuur
Voorkomende reacties
Bij een reactie tussen kaliumnitriet en geconcentreerd salpeterzuur ontstaan kaliumnitraat, stikstofdioxide, stikstofmonoxide en water .
2KNO2 + 2HNO3 = 2KNO3 + NO2 + NO + H2O
Een verzadigde oplossing van KNO2 reageert met geconcentreerd zwavelzuur tot kaliumsulfaat, stikstofdioxide, stikstofmonoxide en water .
2KNO2 + H2SO4 = K2SO4 + NO2 + NO + H2O
Kaliumnitriet reageert met geconcentreerd zoutzuur tot kaliumnitraat, kaliumchloride, salpeteroxide en water .
3KNO2 + 2HCl = KNO3 + 2KCl + 2NO + H2O
Kaliumnitriet toepassingen
- Om andere chemicaliën, warmteoverdracht zouten te maken .
- In chemische analyse .
- Als levensmiddelenadditief (conserveermiddel), in meststoffen .
- Als een tegengif voor cyanide vergiftiging .
- Als vasodilatator op medisch gebied .
- Als antikalkmiddel en corrosieremmer .
Is het gevaarlijk
Het is een vergif als het wordt ingenomen. Het kan explosiegevaar veroorzaken bij verhitting. De verbinding begint te ontbinden bij 350°C en stoot giftige dampen van kaliumoxide uit. KNO2 in voedsel kan het risico op kanker verhogen.
Kaliumnitriet Prijs
10 gram van de verbinding kost rond de $19.2 .
- Potassium Nitrite – Pubchem.ncbi.nlm.nih.gov
- Potassium Nitrite – Chemspider.com
- Wat is de pH van een 0,25M oplossing van kaliumnitriet? – Quora.com
- Kaliumnitriet – Chemicalbook.com
- Bereiding van kaliumnitriet – Prepchem.com
- Kaliumnitriet – Chemicalbook.com
- Kaliumnitriet reageren met salpeterzuur – Chemiday.com
- Kaliumnitriet reageren met zwavelzuur – Chemiday.com
- Kaliumnitriet reageren met waterstofchloride – Chemiday.com