O desafio de gerir uma erupção cutânea cetuximab
Anticorpos receptores do factor de crescimento da epiderme (EGFR) como o cetuximab foram aprovados para uso como gestão de primeira linha, bem como terapia de salvamento para a cabeça e pescoço e cancros colorrectais. Entre a toxicidade esperada mais comum é uma erupção cutânea descrita como acneiforme. A presença de uma erupção cutânea foi postulada para prever um resultado de tratamento mais favorável para os cânceres de cabeça e pescoço1, mas não para o colorectum.2 Com reações medicamentosas mais severas, os pacientes podem requerer uma interrupção do tratamento, o que tem mostrado reduzir o controle locorregional e a sobrevivência, particularmente em pacientes com câncer de cabeça e pescoço.3 Isto tem levado os clínicos a afetar a terapia rápida para reverter a erupção do medicamento. Dada a controvérsia em torno da reversão rápida e eficaz desta reacção medicamentosa, este relatório pretende abordar o estado actual do tratamento clínico usando uma vinheta real do paciente.
Apresentação do caso e resumo
O paciente era um homem branco de 57 anos de idade que tinha sido diagnosticado com carcinoma espinocelular cutâneo (CEC) de grau 3, estágio 4 T4N0M1, dos tecidos moles posuriculares direitos, com erosão na mastoide direita e doença metastática comprovada por biópsia envolvendo a fossa supraclavicular contralateral esquerda e pulmões bilaterais. Sua doença tornou-se quimioterápica refratária, e foi encaminhada para terapia local paliativa para a base do crânio. Devido ao tamanho do tumor (4 cm × 5 cm), ele foi considerado para quimioterapia sensibilizante, mas a cisplatina não foi apropriada devido à perda auditiva crônica.4 O paciente foi recomendado para doses sensibilizantes de cetuximab. Este anticorpo EGFR demonstrou oferecer benefícios similares aos observados com cisplatina no manejo definitivo do SCC de cabeça e pescoço.5
A dose padrão de carga de cetuximab foi administrada a 400 mg/m2 por via intravenosa (IV). Na semana seguinte, a dose sensibilizante de 250 mg/m2 intravenosa foi administrada juntamente com a radioterapia diária para os volumes alvo. A dose semanal de cetuximab continuou a ser de 250 mg/m2. A prescrição de radioterapia foi de 6.000 cGy em 200 cGy de frações diárias, abrangendo o volume bruto do tumor conforme identificado em um exame tomográfico computadorizado com cortes de 3 mm. Utilizamos um arranjo de feixe de radioterapia de arco não coplanar, pois este espalha inerentemente a dose sobre um volume maior de tecido normal, ao mesmo tempo em que fornece sua maior dose ao volume bruto do tumor. Como tal, um volume da orofaringe e cavidade oral do paciente foi incluído dentro da dose de radioterapia penumbra. Após receber 3 doses semanais de cetuximab (1 dose de carga e 2 doses semanais de sensibilização) e 2.000 cGy de radioterapia, o paciente desenvolveu uma erupção cutânea robusta de grau 2 delimitada à face, com poucas lesões dispersas na parte superior anterior do tórax. Ele foi atendido no departamento de oncologia médica e foi prescrito doxiciclina 100 mg por via oral duas vezes ao dia e pomada tópica clindamicina 2% duas vezes ao dia.
Na clínica de oncologia por radiação, sua terapia medicamentosa foi manipulada. Sua reação cutânea cetuximab foi de grau 2, manifestada por eritema moderado com descamação úmida não influente. Devido à preocupação de que o paciente desenvolveria candida oral, o que atrasaria ainda mais sua terapia, os antibióticos orais e tópicos foram descontinuados, assim como a prednisona oral. Foi-lhe prescrito um creme de triamcinolona 0,1% para ser aplicado na face e poucas áreas da parede torácica duas vezes por dia e um enxaguamento bucal oncológico para tratar a mucosite precoce não influente. As imagens que o acompanham mostram a extensão da reacção cutânea cetuximab do doente na linha de base antes do início do tratamento (Figura 1), aos 4 dias após a intervenção (Figura 2), e novamente aos 6 dias após a intervenção (Figura 3). O paciente consentiu em ter suas fotografias tiradas e entendeu que elas seriam usadas para fins de publicação educacional e de pesquisa.
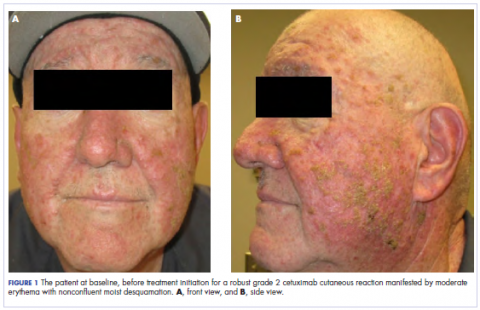
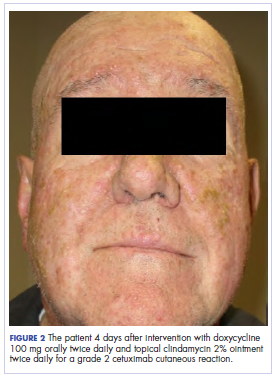
Como se pode ver pelas fotografias, a erupção cutânea do paciente começou a secar e descascar no 4º dia após a intervenção, e não houve novas erupções. O prurido que acompanhava a erupção tinha-se resolvido completamente. No sexto dia, a erupção cutânea tinha diminuído completamente. Devido à resposta ao esteroide tópico, o paciente continuou com o cetuximab sem modificação da dose. Foi-lhe recomendado continuar com o creme de triamcinolona até a conclusão do curso de quimioterapia.
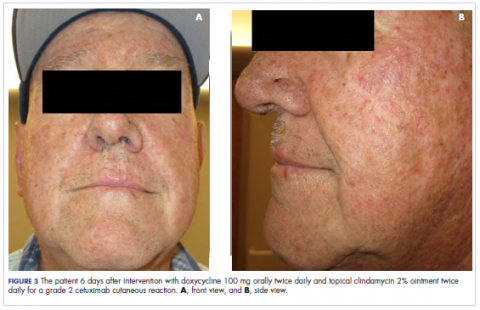
Discussão
Uma erupção cutânea induzida por cetuximab é comum. Em uma meta-análise de 2011 quantificando os graus 1 a 4 de gravidade, cerca de 75% dos pacientes tratados com um inibidor de EGFR experimentaram uma erupção cutânea. A maioria das erupções foi inferior ao grau 3, e a droga foi ou dose-reduzida ou mantida temporariamente, mas geralmente não foi descontinuada.6 É de notar que em uma pesquisa não-selecionada de oncologistas médicos que receitavam cetuximab, 76% relataram manter a droga devido à gravidade da erupção, 60% relataram reduções de dose para uma erupção, e 32% relataram mudar a droga por causa da gravidade da erupção.7
No ensaio inicial de registro farmacêutico, 76% a 88% dos pacientes que receberam cetuximab desenvolveram uma erupção cutânea, 17% dos quais com grau 3, pelo menos. As recomendações farmacêuticas para o tratamento da erupção cutânea incluem um atraso de até 2 semanas para uma erupção de grau 3 ou inferior e para terminar o uso do medicamento se não houver melhora clínica após 2 semanas.8 Biópsias da erupção cutânea confirmam uma reação inflamatória supurativa separada de uma reação acne infecciosa,9 resultando em uma recomendação de tratamento com terapia tópica com esteróides. Em algumas circunstâncias, a reação medicamentosa pode infectar ou envolver a paroníquia, freqüentemente relacionada ao Staphylococcus aureus.10 Apesar do que seria um problema abordado pela terapia médica anti-inflamatória, o aspecto clínico da erupção cutânea marcada por pústulas, juntamente com o relativo estado imunossuprimido de um paciente com câncer, levou os oncologistas médicos a prescreverem terapia antibiótica.
Para abordar os muitos relatórios institucionais únicos sobre o tratamento da erupção cutânea EGFR, várias diretrizes foram publicadas. A primeira diretriz – após um relato de que o cetuximab e a radioterapia simultâneas eram superiores à radioterapia isolada no câncer de cabeça e pescoço localmente avançado, que documentou uma incidência de pelo menos 23% de toxicidade cutânea de grau 3 no braço do cetuximab1 – tentou pontuar a gravidade da erupção cutânea de acordo com os Critérios Terminológicos Comuns para Eventos Adversos (CTCAE) do National Cancer Institute (NCI). Sob esses critérios, os autores definiram a toxicidade de grau 2 como eritema moderado a rápido com descamação úmida desigual, em sua maioria confinada às dobras e dobras cutâneas. A toxicidade de grau 3 foi descrita como umectante úmido que não as dobras e dobras cutâneas com sangramento induzido por trauma menor, e a toxicidade cutânea de grau 4 foi definida como necrose ou ulceração da derme de espessura total com sangramento espontâneo do local envolvido. Os autores passaram a descrever um algoritmo de tratamento relacionado ao grau que incluía lavagem suave da pele, mantendo-a seca e usando agentes anti-inflamatórios tópicos, incluindo esteróides. Os antibióticos devem ser usados na presença de uma suspeita de infecção após o cultivo da área e a toxicidade de grau 4 deve ser encaminhada para um centro de tratamento de feridas.11
Numa declaração de consenso da National Comprehensive Cancer Network, os autores observaram que a maioria das recomendações de manejo foram anedóticas. Eles recomendaram contra o uso de adstringentes e outros agentes secantes, pois exacerbam a dor. A escolha final de esteróides tópicos ou antibióticos foi baseada inteiramente no julgamento subjetivo dada a ausência de dados prospectivos.12
Um relatório de conferência de consenso espanhol argumentou contra qualquer profilaxia contra uma reação cutânea, além de manter a pele limpa e seca.13 Os autores do relatório recomendaram contra a lavagem da pele afetada mais de duas vezes ao dia para evitar o ressecamento excessivo, e defenderam os hidratantes e o desbridamento da crosta cutânea com hidrogel para reduzir a superinfecção e o sangramento.13 Os autores também observaram que algumas diretrizes sugeriram que os esteróides tópicos podem exacerbar uma erupção cutânea,14 mas concluíram que os esteróides tópicos são benéficos desde que sejam usados por menos de duas semanas. Qualquer uso de antibióticos deve ser baseado em evidências claras de uma infecção.13
Na primeira modificação da escala de classificação de erupções cutâneas do NCI, um painel internacional abordou o crescente número de relatos na literatura sugerindo que a escala de toxicidade anterior era possivelmente inadequada em suas recomendações para o tratamento adequado. A escala inicial havia definido apenas a reação cutânea e não qual terapia deveria ser administrada; portanto, na atualização, as descrições para toxicidade de grau 1 e 2 permaneceram inalteradas, mas antibióticos orais foram recomendados para lesão de grau 3, e antibióticos parenterais com enxerto cutâneo foram necessários com toxicidade de grau 4.15
Um painel de especialistas asiáticos sugeriu a modificação da escala de dermatite de bioradiação, definindo uma dermatite de grau 3 como >50% de descamação úmida do campo envolvido com formação de lesões confluentes por causa do tratamento. Eles recomendaram terapia tópica e oral, tratamento de feridas e possível hospitalização em casos graves. O painel sugeriu esteróides tópicos e sistêmicos e antibióticos.16
Finalmente, em um relatório de consenso italiano, os membros modificaram novamente a classificação de toxicidade cutânea e foram notavelmente mais agressivos em termos de suas recomendações de manejo. Eles definiram a toxicidade de grau 2 como pústulas ou pápulas cobrindo 10% a 30% da superfície corporal, com potencial prurido ou ternura. Também notaram o impacto psicossocial das toxinas cutâneas nos pacientes e os limites das suas actividades diárias. Recomendaram creme de vitamina K1 (menadiona), antibióticos tópicos, esteróides tópicos de potência intermediária e antibioticoterapia oral por até 4 semanas para toxicidade de grau 2. Apesar deste tratamento agressivo, os autores admitiram que a utilidade dos esteróides tópicos e dos antibióticos era desconhecida. Eles definiram toxicidade grau 3 como pústulas ou pápulas cobrindo mais de 30% da superfície corporal, com sinais de possível prurido e maciez. Atividades de vida diária e autocuidado foram afetadas, e havia evidência de uma superinfecção. O painel sugeriu o uso de antibióticos enquanto se aguardavam os resultados da cultura, prednisona oral, anti-histamínicos e analgésicos orais. A terapia tópica não foi incluída.17 É notável que apenas o painel italiano recomendou o uso de creme de vitamina K1. Em um estudo prospectivo randomizado, duplo-cego e placebo-controlado fase 2 de 30 pacientes, a menadione não apresentou benefício clínico em termos de redução da gravidade das lesões cutâneas do cetuximab.18
Figure 4 ilustra a nossa abordagem institucional ao tratamento da erupção cutânea cetuximab com base numa combinação das abordagens espanhola e NCI.
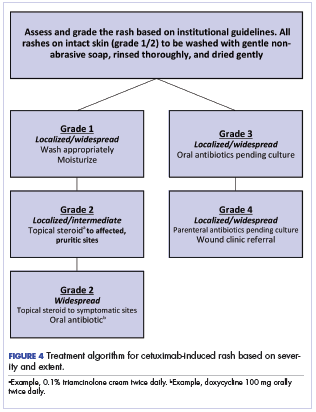
A escolha final da terapia para gerir uma erupção cutânea cetuximab deve ser específica do paciente e do tratamento. Nossa abordagem institucional, como a da série espanhola13 , é evitar a quimioprofilaxia contra uma erupção cutânea; ao contrário, recomendamos a lavagem diária da pele com um sabonete suave seguido de um enxágüe completo e uma secagem adequada e não agressiva. A hidratação da pele intacta demonstrou reduzir a esfoliação, e incorporamos essa abordagem em nosso regime.19
Em nosso paciente, cujo volume do tumor de radioterapia de cabeça e pescoço incluía uma porção da cavidade oral e orofaringe, a antibioticoterapia sistêmica e a terapia com esteróides provavelmente levariam a complicações adicionais com o desenvolvimento da candidíase oral. Portanto, enquanto a gravidade da reação permaneceu em grau 2, pareceu apropriado tratar apenas com esteróides de potência tópicos intermediários e limpeza de pele. Se a reação tivesse se tornado mais severa, então as culturas teriam sido obtidas para orientar nossa decisão sobre a terapia antibiótica. A resposta do nosso paciente aos esteróides tópicos foi previsível e eficaz, e ele foi capaz de prosseguir com o seu curso de terapia do cancro.