Wyzwanie związane z leczeniem wysypki po cetuximabie
Przeciwciała przeciwko receptorowi dla naskórkowego czynnika wzrostu (EGFR), takie jak cetuximab, zostały dopuszczone do stosowania jako leki pierwszego rzutu oraz jako terapia ratunkowa w leczeniu raka głowy i szyi oraz raka jelita grubego. Do najczęstszych spodziewanych objawów toksyczności należy wysypka skórna określana jako trądzikowa. Postuluje się, że obecność wysypki pozwala przewidzieć bardziej korzystny wynik leczenia w przypadku nowotworów głowy i szyi1 , ale nie w przypadku raka jelita grubego.2 W przypadku cięższych reakcji na leki pacjenci mogą wymagać przerwania leczenia, co, jak wykazano, zmniejsza kontrolę lokoregionalną i przeżywalność, szczególnie u pacjentów z nowotworami głowy i szyi.3 Skłoniło to klinicystów do zwrócenia uwagi na szybką terapię mającą na celu odwrócenie objawów wysypki. Biorąc pod uwagę kontrowersje wokół szybkiego i skutecznego odwracania tej reakcji polekowej, niniejsze doniesienie ma na celu omówienie aktualnego stanu zarządzania klinicznego na przykładzie rzeczywistej winiety pacjenta.
Przedstawienie i podsumowanie przypadku
Pacjentem był 57-letni biały mężczyzna, u którego rozpoznano skórnego raka płaskonabłonkowego (SCC) tkanek miękkich prawej okolicy zausznej w stadium 4 T4N0M1 stopnia 3, z nadżerką do prawej kości sutkowej i potwierdzonymi biopsyjnie przerzutami do lewego dołu nadobojczykowego i obu płuc. Jego choroba stała się oporna na chemioterapię i został skierowany na paliatywne leczenie miejscowe do podstawy czaszki. Ze względu na wielkość guza (4 cm × 5 cm) rozważano zastosowanie chemioterapii odczulającej, ale cisplatyna nie była wskazana z powodu przewlekłej utraty słuchu.4 Pacjentowi zalecono odczulające dawki cetuximabu. Wykazano, że to przeciwciało EGFR oferuje podobne korzyści jak cisplatyna w ostatecznym leczeniu SCC głowy i szyi.5
Standardową dawkę obciążającą cetuximabu podano w dawce 400 mg/m2 dożylnie (IV). W następnym tygodniu podawano dawkę odczulającą 250 mg/m2 dożylnie wraz z codzienną radioterapią na objętości docelowe. Tygodniowa dawka cetuximabu nadal wynosiła 250 mg/m2. Zalecono radioterapię w dawce 6000 cGy we frakcjach 200 cGy dziennie, obejmującą objętość guza brutto, określoną w badaniu tomografii komputerowej z 3-mm cięciami. Zastosowaliśmy niekoplanarny układ wiązki radioterapeutycznej, ponieważ w naturalny sposób rozkłada ona dawkę na większą objętość tkanki prawidłowej, jednocześnie dostarczając konformalnie największą dawkę do objętości guza brutto. W związku z tym, objętość gardła i jamy ustnej pacjenta została włączona do penumbry dawki radioterapii. Po otrzymaniu 3 cotygodniowych dawek cetuximabu (1 dawka nasycająca i 2 cotygodniowe dawki uczulające) oraz radioterapii w dawce 2000 cGy, u pacjenta wystąpił silny wykwit skórny 2 stopnia, ograniczony do twarzy, z kilkoma rozproszonymi zmianami w górnej przedniej części klatki piersiowej. Pacjent został przyjęty na oddział onkologii medycznej, gdzie przepisano mu doksycyklinę w dawce 100 mg doustnie dwa razy na dobę oraz miejscowo klindamycynę w maści 2% dwa razy na dobę.
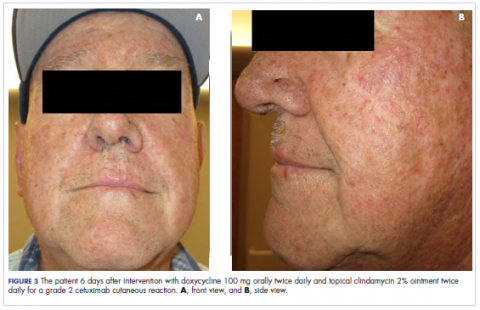
W klinice onkologii radiacyjnej manipulowano jego leczeniem farmakologicznym. Jego reakcja skórna po cetuximabie była stopnia 2, objawiająca się umiarkowanym rumieniem z nierozgałęziającym się wilgotnym łuszczeniem. Z obawy, że u pacjenta rozwinie się candida w jamie ustnej, co dodatkowo opóźniłoby terapię, odstawiono antybiotyki doustne i miejscowe, a także doustny prednizon. Pacjentowi przepisano krem z triamcynolonem 0,1% do stosowania na twarz i kilka obszarów ściany klatki piersiowej dwa razy dziennie oraz onkologiczny płyn do płukania jamy ustnej w celu zaradzenia wczesnemu, nie zlewnemu zapaleniu błony śluzowej. Załączone zdjęcia pokazują zakres reakcji skórnej na cetuximab u pacjenta na poziomie podstawowym przed rozpoczęciem leczenia (Rycina 1), w 4 dni po interwencji (Rycina 2) i ponownie w 6 dni po interwencji (Rycina 3). Pacjent wyraził zgodę na wykonanie zdjęć i zrozumiał, że zostaną one wykorzystane do celów edukacyjnych i publikacji badawczych.
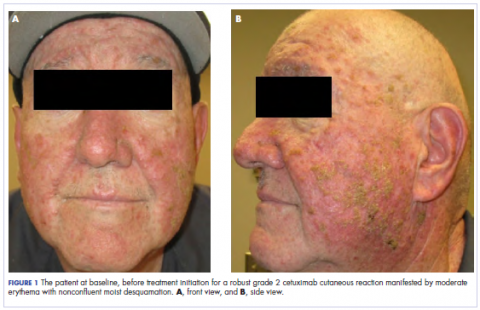
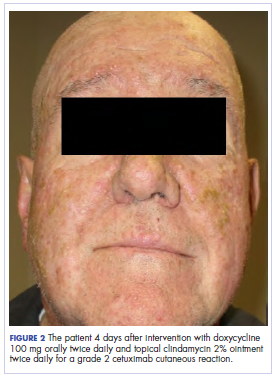
Jak widać na zdjęciach, wysypka u pacjenta zaczęła wysychać i łuszczyć się w 4. dniu po interwencji i nie pojawiły się nowe wykwity. Świąd towarzyszący wysypce całkowicie ustąpił. Do 6. dnia wysypka całkowicie ustąpiła. Ze względu na odpowiedź na steroid miejscowy, pacjent kontynuował leczenie cetuximabem bez modyfikacji dawki. Zalecono mu kontynuację stosowania kremu z triamcynolonem do czasu zakończenia kursu chemioradioterapii.
Dyskusja
Wysypka wywołana cetuximabem występuje często. W metaanalizie z 2011 roku, w której oceniano stopień ciężkości od 1 do 4, wysypka wystąpiła u około 75% pacjentów leczonych inhibitorem EGFR. Większość wysypek miała nasilenie mniejsze niż stopień 3, a lek był zmniejszany pod względem dawki lub czasowo wstrzymywany, ale na ogół nie był odstawiany.6 Na uwagę zasługuje fakt, że w niewyselekcjonowanym badaniu ankietowym przeprowadzonym wśród onkologów medycznych przepisujących cetuksymab 76% zgłosiło wstrzymanie podawania leku z powodu nasilenia wysypki, 60% zgłosiło zmniejszenie dawki z powodu wysypki, a 32% zgłosiło zmianę leku z powodu nasilenia wysypki.7
W początkowym farmaceutycznym badaniu rejestracyjnym u 76% do 88% pacjentów, którzy otrzymywali cetuksymab, wystąpiła wysypka, z czego u 17% wysypka miała co najmniej stopień 3. Zalecenia farmaceutyczne dotyczące postępowania w przypadku wysypki polekowej obejmują opóźnienie podawania leku o maksymalnie 2 tygodnie w przypadku wysypki stopnia 3 lub mniejszego oraz przerwanie stosowania leku, jeśli po 2 tygodniach nie nastąpi poprawa kliniczna.8 Biopsja wysypki potwierdza ropną reakcję zapalną odrębną od zakaźnej reakcji trądzikowej,9 co skutkuje zaleceniem leczenia miejscową steroidoterapią. W niektórych okolicznościach reakcja polekowa może ulec zakażeniu lub objąć paronychię, często związaną z Staphylococcus aureus.10 Pomimo tego, co w innych okolicznościach byłoby problemem rozwiązywanym przez przeciwzapalną terapię medyczną, kliniczny wygląd wysypki naznaczonej krostami, w połączeniu ze względnym stanem immunosupresji u chorego na nowotwór, skłonił onkologów medycznych do przepisania antybiotykoterapii.
Aby odnieść się do wielu pojedynczych doniesień instytucjonalnych dotyczących postępowania w przypadku wysypki EGFR, opublikowano kilka wytycznych. W najwcześniejszych wytycznych – po opublikowaniu doniesienia o przewadze jednoczesnego stosowania cetuximabu i radioterapii nad samą radioterapią w miejscowo zaawansowanym raku głowy i szyi, w którym udokumentowano 23-procentową częstość występowania toksyczności skórnej co najmniej 3. stopnia w ramieniu z cetuximabem1 – podjęto próbę oceny nasilenia wysypki zgodnie z opracowanymi przez National Cancer Institute (NCI) Common Terminology Criteria for Adverse Events (CTCAE). Zgodnie z tymi kryteriami autorzy zdefiniowali toksyczność stopnia 2 jako umiarkowany do szybkiego rumień z plamistym, wilgotnym łuszczeniem, ograniczonym głównie do fałdów skórnych i zagnieceń. Toksyczność stopnia 3 została opisana jako wilgotne łuszczenie poza fałdami skórnymi i fałdami z krwawieniem wywołanym niewielkim urazem, a toksyczność skórna stopnia 4 została zdefiniowana jako martwica skóry lub owrzodzenie skóry właściwej o pełnej grubości z samoistnym krwawieniem z miejsca objętego badaniem. Autorzy opisali algorytm leczenia w zależności od stopnia, który obejmował delikatne mycie skóry, utrzymywanie jej w suchości oraz stosowanie miejscowych środków przeciwzapalnych, w tym steroidów. Antybiotyki należy stosować w przypadku podejrzenia zakażenia po uprzednim wyhodowaniu miejsca, a toksyczność stopnia 4 powinna być skierowana do centrum leczenia ran.11
W konsensusie National Comprehensive Cancer Network autorzy zauważyli, że większość zaleceń dotyczących postępowania jest niepotwierdzona. Odradzali stosowanie środków ściągających i innych środków wysuszających, ponieważ nasilają one ból. Ostateczny wybór miejscowych steroidów lub antybiotyków opierał się całkowicie na subiektywnej ocenie z uwagi na brak danych prospektywnych.12
W hiszpańskim raporcie z konferencji konsensusowej opowiedziano się przeciwko jakiejkolwiek profilaktyce reakcji skórnej, poza utrzymywaniem skóry w czystości i suchości.13 Autorzy raportu zalecili, aby nie myć zmienionej chorobowo skóry częściej niż dwa razy dziennie, aby uniknąć nadmiernego wysuszenia, oraz opowiedzieli się za stosowaniem środków nawilżających i usuwaniem zaskorupień skóry za pomocą hydrożeli w celu zmniejszenia nadkażenia i krwawienia.13 Autorzy zauważyli również, że niektóre wytyczne sugerują, iż miejscowe steroidy mogą nasilać wysypkę,14 ale doszli do wniosku, że miejscowe steroidy są korzystne, o ile są stosowane krócej niż 2 tygodnie. Każde zastosowanie antybiotyków powinno być oparte na wyraźnych dowodach zakażenia.13
W pierwszej modyfikacji skali klasyfikacji wysypek CTCAE NCI, międzynarodowy panel zajął się rosnącą liczbą doniesień w literaturze sugerujących, że poprzednia skala toksyczności była prawdopodobnie nieadekwatna w swoich zaleceniach dotyczących odpowiedniego leczenia. Pierwotna skala definiowała jedynie reakcję skórną, a nie to, jaką terapię należy zastosować; dlatego w aktualizacji opisy toksyczności stopnia 1 i 2 pozostały niezmienione, ale w przypadku zmian stopnia 3 zalecono doustne antybiotyki, a w przypadku toksyczności stopnia 4 konieczne było zastosowanie antybiotyków pozajelitowych z przeszczepem skóry.15
Azjatycki panel ekspertów zaproponował modyfikację skali bioradiacyjnego zapalenia skóry, definiując stopień 3 zapalenia skóry jako >50% wilgotnego złuszczania się skóry w obszarze objętym działaniem promieniowania z tworzeniem się zlewnych zmian z powodu leczenia. Zalecono zarówno leczenie miejscowe, jak i doustne, pielęgnację ran, a w ciężkich przypadkach ewentualną hospitalizację. Panel sugerował stosowanie steroidów miejscowych i ogólnoustrojowych oraz antybiotyków.16
W końcu, we włoskim raporcie konsensusu, członkowie ponownie zmodyfikowali klasyfikację toksyczności skórnej i byli znacznie bardziej agresywni w zakresie zaleceń dotyczących postępowania. Zdefiniowali oni toksyczność stopnia 2 jako krosty lub grudki obejmujące od 10% do 30% powierzchni ciała, z potencjalnym świądem lub tkliwością. Zwrócili również uwagę na psychospołeczny wpływ toksyczności skórnych na pacjentów i ograniczenia w wykonywaniu przez nich codziennych czynności życiowych. W przypadku toksyczności stopnia 2. zalecili stosowanie kremu z witaminą K1 (menadion), miejscowych antybiotyków, miejscowych steroidów o pośredniej sile działania oraz doustnej antybiotykoterapii przez okres do 4 tygodni. Pomimo tak agresywnego przebiegu leczenia autorzy przyznali, że przydatność miejscowego stosowania steroidów i antybiotyków nie jest znana. Toksyczność stopnia 3. zdefiniowali jako krostki lub grudki obejmujące ponad 30% powierzchni ciała, z objawami możliwego świądu i tkliwości. Czynności życia codziennego i samoopieka były zaburzone, a ponadto istniały dowody na superinfekcję. Panel sugerował stosowanie antybiotyków w oczekiwaniu na wyniki posiewu, doustnego prednizonu, leków przeciwhistaminowych i doustnych leków przeciwbólowych. Nie uwzględniono terapii miejscowej.17 Warto zauważyć, że tylko włoski panel zalecił stosowanie kremu z witaminą K1. W prospektywnym randomizowanym, podwójnie zaślepionym, kontrolowanym placebo badaniu fazy 2 z udziałem 30 pacjentów menadion nie wykazywał korzyści klinicznych w zakresie zmniejszenia nasilenia zmian skórnych wywołanych przez cetuximab.18
Rycina 4 przedstawia nasze instytucjonalne podejście do leczenia wysypki wywołanej cetuksymabem oparte na połączeniu podejścia hiszpańskiego i NCI.
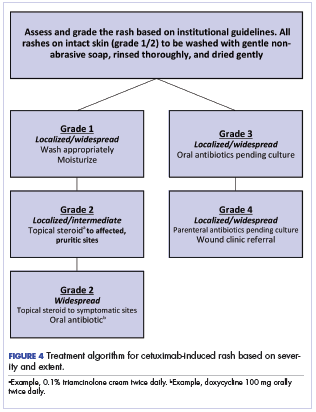
Ostateczny wybór terapii w celu opanowania wysypki wywołanej cetuksymabem musi być uzależniony od pacjenta i sposobu leczenia. Nasze podejście instytucjonalne, podobnie jak w serii hiszpańskiej,13 polega na unikaniu chemioprofilaktyki przeciw wysypce; zalecamy raczej codzienne mycie skóry delikatnym mydłem, a następnie dokładne spłukiwanie i odpowiednie, nieagresywne osuszanie. Wykazano, że nawilżanie nieuszkodzonej skóry zmniejsza złuszczanie i włączyliśmy to podejście do naszego schematu postępowania.19
W przypadku naszego pacjenta, u którego objętość guza po radioterapii głowy i szyi obejmowała część jamy ustnej i gardła, ogólnoustrojowa antybiotykoterapia i steroidoterapia prawdopodobnie doprowadziłaby do dalszych komplikacji związanych z rozwojem kandydozy jamy ustnej. Dlatego też, mimo że nasilenie reakcji pozostało na poziomie stopnia 2, właściwe wydawało się leczenie jedynie miejscowymi steroidami o średniej sile działania i oczyszczanie skóry. Gdyby reakcja stała się bardziej nasilona, należałoby pobrać posiewy w celu podjęcia decyzji o antybiotykoterapii. Odpowiedź naszego pacjenta na miejscowe steroidy była przewidywalna i skuteczna, a on sam mógł kontynuować leczenie przeciwnowotworowe.