22.8: Reactivity of Enolate Ions
General Reaction of Enolates
Since the negative charge of anion enolate is delocalized over the alfa-carbon and the oxygen, electrophiles may bond to either atom. Reaktanty posiadające dwa lub więcej miejsc reaktywnych są nazywane ambidentami, więc termin ten jest właściwie stosowany do anionów enolanowych. Umiarkowanie elektrofilowe reagenty, takie jak halogenki alkilowe, nie są wystarczająco reaktywne, aby łączyć się z obojętnymi tautomeriami enolowymi, ale zwiększona nukleofilowość zasady sprzęgającej anion enolanowy pozwala na zachodzenie takich reakcji. Ponieważ alkilacje są zwykle nieodwracalne, ich produkty powinny odzwierciedlać nieodłączną (kinetyczną) reaktywność różnych miejsc nukleofilowych.
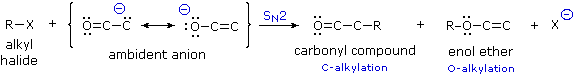
Jeśli halogenek alkilowy ulega reakcji SN2 przy atomie węgla anionu enolanowego, produktem jest alkilowany aldehyd lub keton. Z drugiej strony, jeżeli reakcja SN2 zachodzi przy tlenie, produktem jest pochodna eterowa tautomeru enolowego; takie związki są stabilne w nieobecności kwasu i mogą być izolowane i charakteryzowane. Te alkilacje (przedstawione powyżej) są nieodwracalne w warunkach zwykle stosowanych w reakcjach SN2, tak więc skład produktu powinien dostarczyć miary względnej szybkości podstawienia przy węglu w stosunku do tlenu. Stwierdzono, że ta konkurencja jest wrażliwa na szereg czynników, w tym gęstość ładunku ujemnego, solwatację, koordynację kationów i stabilność produktu.
.