La sfida di gestire un rash da cetuximab
Gli anticorpi del recettore del fattore di crescita epidermico (EGFR) come il cetuximab sono stati approvati per l’uso come gestione di prima linea e come terapia di salvataggio per i tumori di testa e collo e colorettali. Tra le tossicità attese più comuni c’è un’eruzione cutanea descritta come acneiforme. La presenza di un’eruzione cutanea è stata postulata per predire un esito più favorevole del trattamento per i tumori della testa e del collo1 ma non per il colon-retto.2 Con reazioni al farmaco più gravi, i pazienti possono richiedere un’interruzione del trattamento, che ha dimostrato di ridurre il controllo locoregionale e la sopravvivenza, in particolare nei pazienti con cancro della testa e del collo.3 Ciò ha spinto i medici a interessare una terapia rapida per invertire l’eruzione del farmaco. Data la controversia intorno all’inversione rapida ed efficace di questa reazione al farmaco, questo rapporto mira ad affrontare lo stato attuale della gestione clinica utilizzando una vignetta del paziente reale.
Presentazione del caso e riassunto
Il paziente era un uomo bianco di 57 anni a cui era stato diagnosticato un carcinoma squamocellulare cutaneo (SCC) di grado 3 al quarto stadio T4N0M1 dei tessuti molli postauricolari destri, con erosione nella mastoide destra e malattia metastatica provata da biopsia che coinvolgeva la fossa sopraclavicolare sinistra controlaterale e i polmoni bilaterali. La sua malattia è diventata refrattaria alla chemioterapia, ed è stato indirizzato per una terapia locale palliativa alla base del cranio. A causa delle dimensioni del tumore (4 cm × 5 cm), è stato considerato per la chemioterapia sensibilizzante, ma il cisplatino non era appropriato a causa della perdita cronica dell’udito.4 Al paziente sono state raccomandate dosi sensibilizzanti di cetuximab. Questo anticorpo EGFR ha dimostrato di offrire benefici simili a quelli osservati con il cisplatino nella gestione definitiva del SCC di testa e collo.5
La dose di carico standard di cetuximab è stata somministrata a 400 mg/m2 per via endovenosa (IV). La settimana successiva, la dose di sensibilizzazione di 250 mg/m2 IV è stata somministrata insieme alla radioterapia quotidiana ai volumi bersaglio. La dose settimanale di cetuximab continuò a 250 mg/m2. La prescrizione della radioterapia era di 6.000 cGy in frazioni giornaliere di 200 cGy, comprendendo il volume lordo del tumore come identificato su una scansione computerizzata-tomografica con tagli di 3 mm. Abbiamo usato una disposizione del fascio di radioterapia ad arco non coplanare perché intrinsecamente diffonde la dose su un volume più grande di tessuto normale mentre conformamente consegna la sua dose più grande al volume lordo del tumore. Come tale, un volume dell’orofaringe e della cavità orale del paziente è stato incluso nella penombra della dose di radioterapia. Dopo aver ricevuto 3 dosi settimanali di cetuximab (1 dose di carico e 2 dosi settimanali di sensibilizzazione) e 2.000 cGy di radioterapia, il paziente ha sviluppato una robusta eruzione cutanea di grado 2 delimitata al viso, con poche lesioni sparse sulla parte superiore anteriore del petto. È stato visto nel reparto di oncologia medica e gli è stata prescritta la doxiciclina 100 mg per via orale due volte al giorno e la clindamicina topica 2% in pomata due volte al giorno.
Nella clinica di radio-oncologia, la sua terapia farmacologica è stata manipolata. La sua reazione cutanea al cetuximab era di grado 2, manifestata da un eritema moderato con desquamazione umida non confluente. A causa della preoccupazione che il paziente potesse sviluppare una candida orale, che avrebbe ulteriormente ritardato la sua terapia, gli antibiotici orali e topici furono sospesi, così come il prednisone orale. Gli è stata prescritta una crema al triamcinolone 0,1% da applicare sul viso e su alcune aree della parete toracica due volte al giorno e un colluttorio oncologico per affrontare la mucosite precoce non confluente. Le immagini allegate mostrano l’estensione della reazione cutanea al cetuximab del paziente al basale prima dell’inizio del trattamento (Figura 1), a 4 giorni dopo l’intervento (Figura 2), e di nuovo a 6 giorni dopo l’intervento (Figura 3). Il paziente ha acconsentito a farsi fotografare e ha capito che sarebbero state usate per scopi educativi e di pubblicazione della ricerca.
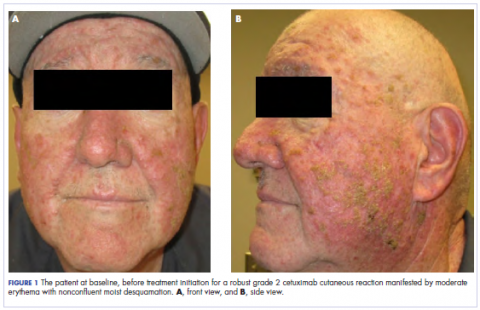
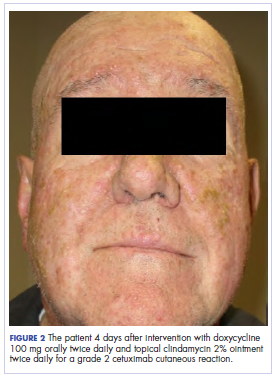
Come si può vedere dalle fotografie, l’eruzione cutanea del paziente ha cominciato a seccarsi e a spellarsi il quarto giorno dopo l’intervento, e non ci sono state nuove eruzioni. Il prurito che accompagnava l’eruzione si era completamente risolto. Al 6° giorno, l’eruzione era completamente scomparsa. A causa della risposta allo steroide topico, il paziente ha continuato il cetuximab senza una modifica della dose. Gli è stato raccomandato di continuare con la crema al triamcinolone fino alla conclusione del corso di chemioradioterapia.
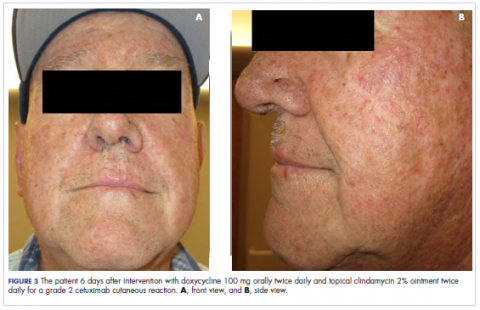
Discussione
Un rash indotto dal cetuximab è comune. In una meta-analisi del 2011 che quantifica i gradi da 1 a 4 di gravità, circa il 75% dei pazienti trattati con un inibitore EGFR ha sperimentato un rash. La maggior parte delle eruzioni cutanee erano di grado inferiore a 3 e il farmaco è stato ridotto o temporaneamente sospeso, ma non è stato generalmente interrotto.6 Da notare che in un’indagine non selezionata di oncologi medici che prescrivevano cetuximab, il 76% ha riferito di aver sospeso il farmaco a causa della gravità dell’eruzione cutanea, il 60% ha riferito di aver ridotto la dose per un’eruzione cutanea e il 32% ha riferito di aver cambiato il farmaco a causa della gravità dell’eruzione cutanea.7
Nello studio iniziale di registrazione farmaceutica, dal 76% all’88% dei pazienti che hanno ricevuto cetuximab hanno sviluppato un rash, il 17% dei quali erano almeno di grado 3. Le raccomandazioni farmaceutiche per la gestione del rash da farmaco includono un ritardo del farmaco fino a 2 settimane per un rash di grado 3 o inferiore e di interrompere l’uso del farmaco se non c’è miglioramento clinico dopo 2 settimane.8 Le biopsie del rash confermano una reazione infiammatoria suppurativa separata da una reazione infettiva dell’acne,9 con conseguente raccomandazione di trattare con una terapia steroidea topica. In alcune circostanze, la reazione farmacologica può infettarsi o coinvolgere la paronichia, spesso legata allo Staphylococcus aureus.10 Nonostante quello che altrimenti sarebbe un problema affrontato da una terapia medica antinfiammatoria, l’aspetto clinico dell’eruzione cutanea caratterizzata da pustole, unito al relativo stato immunosoppresso di un paziente oncologico, ha spinto gli oncologi medici a prescrivere una terapia antibiotica.
Per affrontare i molti rapporti di singole istituzioni sulla gestione dell’eruzione EGFR, sono state pubblicate diverse linee guida. La prima linea guida – dopo un rapporto secondo il quale il cetuximab e la radioterapia concomitanti erano superiori alla sola radioterapia nel cancro della testa e del collo localmente avanzato, che documentava un’incidenza del 23% di tossicità cutanea di almeno grado 3 nel braccio cetuximab1 – ha tentato di assegnare un punteggio alla gravità dell’eruzione cutanea secondo i Common Terminology Criteria for Adverse Events (CTCAE) del National Cancer Institute (NCI). Secondo questi criteri, gli autori hanno definito la tossicità di grado 2 come eritema da moderato a vivace con desquamazione umida a chiazze, per lo più confinata alle pieghe della pelle. La tossicità di grado 3 è stata descritta come desquamazione umida diversa da pieghe e pieghe della pelle con sanguinamento indotto da un trauma minore, e la tossicità cutanea di grado 4 è stata definita come necrosi della pelle o ulcerazione del derma a tutto spessore con sanguinamento spontaneo dal sito coinvolto. Gli autori hanno continuato a descrivere un algoritmo di trattamento legato al grado che includeva il lavaggio delicato della pelle, il mantenimento dell’asciutto e l’uso di agenti antinfiammatori topici, compresi gli steroidi. Gli antibiotici dovrebbero essere usati in presenza di una sospetta infezione dopo la coltura dell’area, e la tossicità di grado 4 dovrebbe essere riferita a un centro di cura delle ferite.11
In una dichiarazione di consenso del National Comprehensive Cancer Network, gli autori hanno notato che la maggior parte delle raccomandazioni di gestione sono aneddotiche. Hanno raccomandato di non usare astringenti e altri agenti essiccanti perché esacerbano il dolore. La scelta finale di steroidi topici o antibiotici era basata interamente sul giudizio soggettivo, data l’assenza di dati prospettici.12
Un rapporto di una conferenza di consenso spagnola si è espresso contro qualsiasi profilassi contro una reazione cutanea, oltre a mantenere la pelle pulita e asciutta.13 Gli autori del rapporto hanno raccomandato di non lavare la pelle colpita più di due volte al giorno per evitare un’eccessiva asciugatura, e hanno raccomandato l’uso di idratanti e lo sbrigliamento delle croste cutanee con idrogeli per ridurre la superinfezione e il sanguinamento.13 Gli autori hanno anche notato che alcune linee guida hanno suggerito che gli steroidi topici potrebbero esacerbare un’eruzione cutanea,14 ma hanno concluso che gli steroidi topici sono benefici finché sono usati per meno di 2 settimane. Qualsiasi uso di antibiotici dovrebbe essere basato sulla chiara evidenza di un’infezione.13
Nella prima modifica della scala di classificazione CTCAE del NCI, un gruppo internazionale ha affrontato il crescente numero di rapporti in letteratura che suggerivano che la precedente scala di tossicità era probabilmente inadeguata nelle sue raccomandazioni per un trattamento appropriato. La scala iniziale aveva definito solo la reazione cutanea e non la terapia da somministrare; pertanto, nell’aggiornamento, le descrizioni per i gradi 1 e 2 di tossicità sono rimaste invariate, ma sono stati raccomandati antibiotici orali per le lesioni di grado 3, e antibiotici parenterali con innesto cutaneo sono stati richiesti con tossicità di grado 4.15
Un gruppo di esperti asiatici ha suggerito di modificare la scala della dermatite da bioradiazioni, definendo una dermatite di grado 3 come >50% desquamazione umida del campo coinvolto con formazione di lesioni confluenti a causa del trattamento. Hanno raccomandato una terapia sia topica che orale, la cura delle ferite e un possibile ricovero nei casi gravi. Il gruppo ha suggerito steroidi topici e sistemici e antibiotici.16
Infine, in un rapporto di consenso italiano, i membri hanno nuovamente modificato la classificazione della tossicità cutanea e sono stati notevolmente più aggressivi in termini di raccomandazioni di gestione. Hanno definito la tossicità di grado 2 come pustole o papule che coprono dal 10% al 30% della superficie corporea, con potenziale prurito o tenerezza. Hanno anche notato l’impatto psicosociale delle tossicità cutanee sui pazienti e i limiti alle loro attività della vita quotidiana. Hanno raccomandato una crema alla vitamina K1 (menadione), antibiotici topici, steroidi topici a potenza intermedia e una terapia antibiotica orale fino a 4 settimane per la tossicità di grado 2. Nonostante questo trattamento aggressivo, gli autori ammisero che l’utilità degli steroidi e degli antibiotici topici era sconosciuta. Hanno definito la tossicità di grado 3 come pustole o papule che coprono più del 30% della superficie corporea, con segni di possibile prurito e tenerezza. Le attività della vita quotidiana e la cura di sé erano influenzate, e c’era evidenza di una superinfezione. Il panel ha suggerito l’uso di antibiotici in attesa dei risultati della coltura, prednisone orale, antistaminici e analgesici orali. La terapia topica non è stata inclusa.17 È degno di nota il fatto che solo il panel italiano ha raccomandato l’uso della crema alla vitamina K1. In uno studio prospettico di fase 2 randomizzato, in doppio cieco e controllato con placebo su 30 pazienti, il menadione non ha mostrato alcun beneficio clinico in termini di riduzione della gravità delle lesioni cutanee da cetuximab.18
La figura 4 illustra il nostro approccio istituzionale al trattamento del rash da cetuximab basato su una combinazione degli approcci spagnolo e NCI.
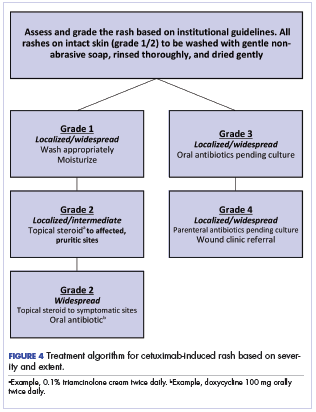
La scelta definitiva della terapia per gestire un rash da cetuximab deve essere specifica del paziente e del trattamento. Il nostro approccio istituzionale, come quello della serie spagnola,13 è di evitare la chemioprofilassi contro l’eruzione cutanea; piuttosto, raccomandiamo il lavaggio quotidiano della pelle con un sapone delicato seguito da un risciacquo accurato e un’asciugatura adeguata e non aggressiva. Idratare la pelle intatta ha dimostrato di ridurre l’esfoliazione, e noi abbiamo incorporato questo approccio nel nostro regime.19
Nel nostro paziente, il cui volume tumorale da radioterapia di testa e collo includeva una parte della cavità orale e dell’orofaringe, la terapia antibiotica e steroidea sistemica avrebbe probabilmente portato a ulteriori complicazioni con lo sviluppo della candidosi orale. Pertanto, mentre la gravità della reazione rimaneva un grado 2, sembrava appropriato trattare solo con steroidi topici di potenza intermedia e pulizia della pelle. Se la reazione fosse diventata più grave, si sarebbero ottenute delle colture per guidare la nostra decisione sulla terapia antibiotica. La risposta del nostro paziente agli steroidi topici era prevedibile ed efficace, ed è stato in grado di procedere con il suo corso di terapia del cancro.